
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
Издательство: Просвещение
Тип: Учебник
§ 2. Тепловые эффекты химических реакций
Вопросы и задания
1. Составьте краткий план-конспект параграфа.
План-конспект параграфа:
- Химические реакции по тепловому эффекту делятся на экзотермические и эндотермические.
- Экзотермические реакции — реакции с выделением тепла (горение природного газа). Выделение теплоты условно обозначается: +Q.
- Эндотермические реакции — реакции с поглощением теплоты (обжиг известняка). Поглощение теплоты условно обозначается: -Q.
- Уравнения химических реакций, которые идут с тепловым эффектом, называются термохимическими уравнениями.
- В термохимических уравнениях необходимо обязательно указывать агрегатное состояние вещества.
- Закон сохранения и поглощения энергии: выделяющаяся при химических реакциях энергия может быть преобразована в другие виды энергии.
2. Какие данные нужно обязательно указывать при составлении термохимических уравнений? Поясните на конкретных примерах.
При составлении термохимических реакций необходимо указывать термохимическое состояние вещества: газообразное (г.), твёрдое (т.), жидкое (ж.), в зависимости от теплового эффекта (экзотермическая или эндотермическая реакция) ставится знак + или -.
CaO(т)+H2O(ж)→СaOH2(т)+Q
2HgO(тв)→2Hg(ж)+O2(г)-Q
3. Какое количество теплоты выделится при сжигании 100 л водорода, взятого при нормальных условиях, в избытке кислорода? Термохимическое уравнение реакции: 2Н2(г.) + 02(г.) = 2Н2o(г.) + 484 кДж
2Н2(г.) + 02(г.) = 2Н2o(г.) + 484 кДж
![]()
|
На количество вещества |
4,46 моль |
х кДж |
|
На один моль |
2 молекулы |
+484 кДж |
х=4,46*484/2=1080,35 кДж
Ответ: 1090,35 кДж.
4. Вычислите, сколько сгорело угля, если при этом выделилось 33 520 кДж теплоты.
С(тв)+O2(г)→СO2(г)+402,24 кДж
Q=33520 кДж
|
На количество вещества |
х моль |
33520 кДж |
|
На один моль |
1 молекула |
+4о2,24 кДж |
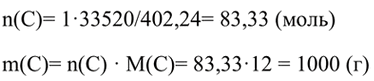
Ответ: 1000 г.
Выберите параграф
