
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
Издательство: Просвещение
Тип: Учебник
§ 11. Практическая работа №2.
Решение экспериментальных задач по теме “Свойства кислот, оснований и солей как электролитов”
1. Вариант 1. Налейте в пробирку 1—2 мл разбавленной 1 :4 серной кислоты и опустите в нее кусочек цинка. Составьте уравнение реакции в молекулярном, ионном и сокращённом ионном виде, покажите переход электронов и объясните, что в этой реакции является окислителем.
Вариант 2. Налейте в пробирку 1—2 мл соляной кислоты и опустите в неё несколько стружек магния. Составьте уравнение реакции в молекулярном, ионном и сокращённом ионном виде, покажите переход электронов и объясните, что в этой реакции является окислителем.

2. Вариант I. В трёх пробирках дан раствор хлорида магния. В первую пробирку прилейте раствор гидроксила натрия, во вторую — карбоната натрия, в третью — нитрата цинка. Составьте уравнения реакций, идущих до конца, в молекулярном, ионном и сокращённом ионном виде.
Вариант 2. В трёх пробирках дан раствор хлорида магния. В первую пробирку прилейте раствор фосфата калия, во вторую — сульфида натрия, в третью — нитрата калия. Составьте уравнения реакций, идущих до конца, в молекулярном, ионном и сокращённом ионном виде.

3. Вариант 1. Даны растворы: а) карбоната калия и соляной кислоты; б) сульфида натрия и серной кислоты; в) хлорида цинка и азотной кислоты. Слейте попарно эти растворы, осторожно понюхайте и определите, в каких случаях реакции идут до конца и почему. Составьте уравнения соответствующих реакций в молекулярном, ионном и сокращённом ионном виде.
Вариант 2. Даны растворы: а) сульфита натрия и соляной кислоты; б) сульфата меди(II) и азотной кислоты; в) карбоната натрия и серной кислоты. Слейте попарно эти растворы, осторожно понюхайте и определите, в каких случаях реакции идут до конца и почему. Составьте уравнения соответствующих реакций в молекулярном, ионном и сокращённом ионном виде.

4. Вариант 1. Осуществите реакции, соответствующие сокращённым ионным уравнениям:
а) Са2+ + СО(2-/3) = СаСО3
б) SO(2-/3) + 2Н+ = SO2 + Н2O
в) ОН- + Н+ = Н2О
Вариант 2. Осуществите реакции, соответствующие сокращённым ионным уравнениям:
а) Fe3+ + ЗOН- = Fe(OH)3
б) СО(2-/3)+ 2Н+ = СO2 + Н2O
в) Ag+ + Сl- = AgCl
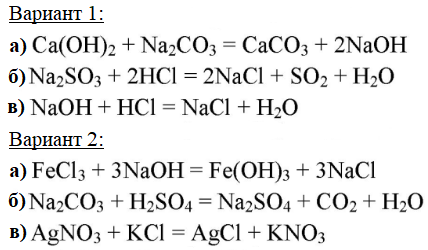
5. Вариант 1. Пользуясь растворами, находящимися на столе, получите: а) гидроксид железа(III); б) сульфид меди(II). Составьте молекулярные, ионные и сокращённые ионные уравнения соответствующих реакций.
Вариант 2. Пользуясь растворами, находящимися на столе, получите: а) оксид cepы(IV); б) карбонат кальция. Составьте молекулярные, ионные и сокращённые ионные уравнения соответствующих реакций.
Отчёт о работе выполните в произвольной форме.
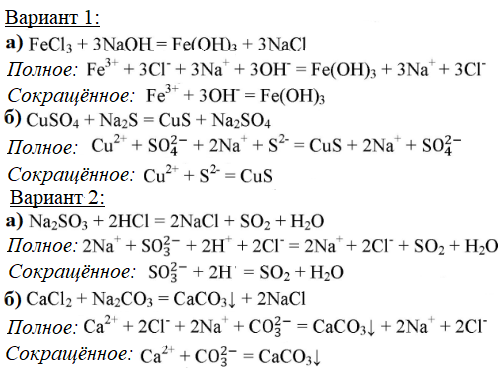
Выберите параграф
