
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
Издательство: Просвещение
Тип: Учебник
§ 15. Соляная кислота и её соли
Вопросы и задания
1. Как в лабораторных условиях и в промышленности получают соляную кислоту? Составьте уравнения соответствующих реакций.
Соляную кислоту получают путём растворения хлороводорода в воде.

2. Даны следующие вещества: Zn, Сu, Al, CaO, SiO2, Fe2O3, NaOH, Аl(OН)3, Fe2(SO4)3, CaCO3, Fe(NO3)3. Какие из этих веществ реагируют с соляной кислотой? Составьте уравнения соответствующих реакций.
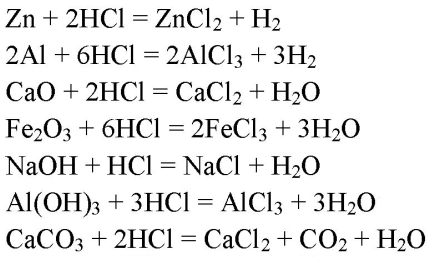
3. Хлороводород, который получили при взаимодействии избытка концентрированной серной кислоты с 58,5 г хлорида натрия, растворили в 146 г воды. Определите массовую долю хлороводорода (в процентах) в полученном растворе.

4. В одном объеме воды при комнатной температуре растворяется примерно 500 объёмов хлороводорода. Вычислите массовую долю хлороводорода (в процентах) в полученном растворе.

5. С помощью компьютера подготовьте реферат на тему «Применение соляной кислоты и её солей».
Производство соляной кислоты было освоено в 1962 году.
Соляная кислота применяется в медицинской, химической, пищевой промышленности. металлургии.
Основные области применения: производство хлористых солей (аммония, бария, цинка), гидрометаллургия платины, золота и серебра, производство уксусной кислоты, органических продуктов. синтетических красителей, активированного угля. гидролизного спирта. дубление и крашение кожи, производство клея, текстильная промышленность, очистка паровых котлов и т.д.
Соли часто используются в производстве и в повседневной жизни:
KCl — удобрение, применяется в стекольной и химической промышленности;
Hg2Cl2 — слабительное средство;
HgCl2 — ядовит, применяется в медицине для дезинфекции;
NaCl (поваренная соль) — используется в кулинарии и консервации, а также в кожевенной и мыловаренной промышленности;
AgCl — применяется в черно-белой фотографии, так как обладает светочувствительностью;
ZnCl2 — используется при паянии, в медицине, для пропитки древесины.
Тестовые задания
1. Установите соответствие между исходными и полученными веществами в уравнениях химических реакций, характеризующих свойства соляной кислоты.
1) НСl + Zn
2) HCI + MgO
3) HCI + Са(ОН)2
4) HCI + AgNO3
A. Mg(OH)2 + Cl2
Б. H2O + CaCl2
B. H2 + ZnCl2
Г. H2O + MgCl2
Д. AgCl + HNO3
- В
- Г
- Б
- Д
2. Различить галогеноводородные кислоты и их соли можно с помощью одного реактива. Этот реактив —
1) хлорная вода
2) нитрат серебра
3) крахмальный клейстер
4) медь
2) нитрат серебра
